正方形の形のp-V グラフから熱効率を求める方法をまとめました。

例題
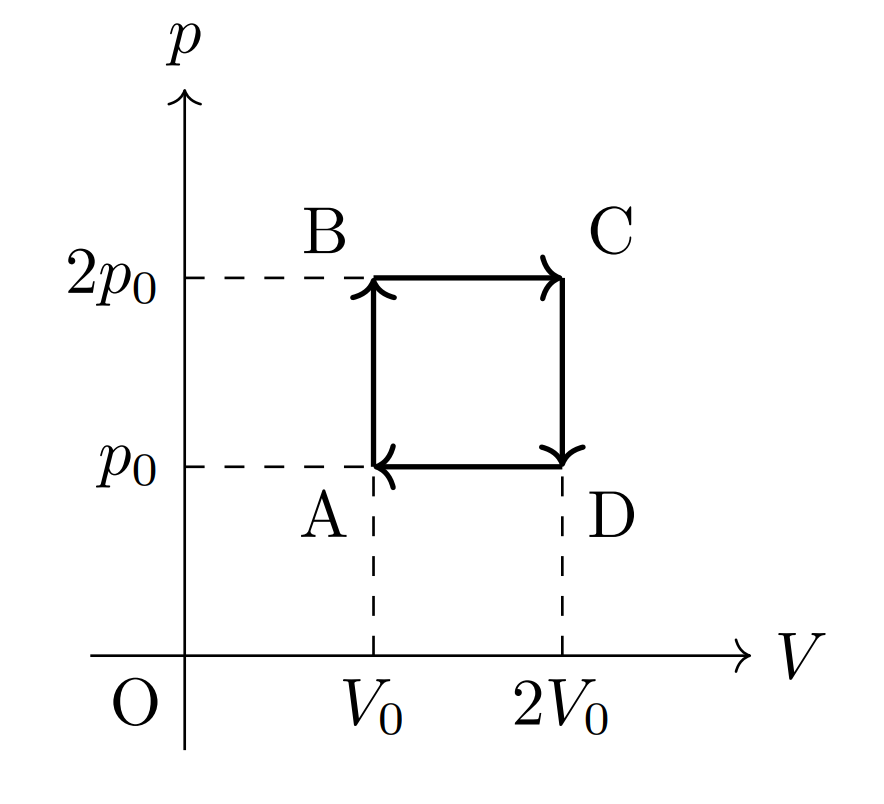
単原子分子からなる理想気体 \(n\) mol を容器に入れ,圧力 \(P\) と体積 \(V\) を A→B→C→D→A のように変化させた。この系の熱効率を求めたい。以下,A の絶対温度を \(T_0\) とし,気体定数を \(R\) とする。
(1) B,C,D の温度を \(T_0\) を用いて表しなさい。
(2) 各過程で気体のする仕事を求め,それらの総和 \(W_{total}\) を求めよ。
(3) 各過程の内部エネルギー変化 \(d U\) を求めよ。
(4) 各過程で気体が熱源から得る熱量を符号も含めて示せ。
(5) この系の熱効率 \(e\) を求めよ。
解答と解説
(1) の考え方
各点における温度はボイル・シャルルの法則 \[\frac{pV}{T}=\text{const}\] を用いることによって求めることが出来ます。この式を使うときには求めたい状態ともう1つ,既知の状態を知っている必要がありますが,ここではAの情報(\(p_0,V_0,T_0\))を使えば良いですね。
【解答】
B,C,Dの温度をそれぞれ \(T_B,T_C,T_D\) とする。ボイル・シャルルの法則より \[\frac{p_0 V_0}{T_0}=\frac{2p_0 V_0}{T_B}\] \[\frac{p_0 V_0}{T_0}=\frac{2p_0 \cdot 2V_0}{T_C}\] \[\frac{p_0 V_0}{T_0}=\frac{p_0 \cdot 2V_0}{T_D}\] これより \[T_B=2T_0,\;T_C=4T_0,\;T_D=2T_0\]
(2) の考え方
各点の温度が求まったら次にこの系( A→B→C→D→A)がする正味の仕事を求めてみましょう。ここで気体のする仕事は \[
dW=p d V
\] で与えられます。ここで,$dV$ は体積 $V$ の変化量を表します。
【解答】
A→Bにおいて,気体は定積変化をしているので \(d V=0\) 。従って \[
W_{AB}=0
\] B→Cにおいて,\(p=2p_0\),\(d V=V_0\) より \[
W_{BC}=2p_0 V_0
\] C→Dにおいて気体は定積変化をしているので \(d V=0\) 。従って \[
W_{CD}=0
\] D→Aにおいて \(p=2p_0\),\(d V=-V_0\) より \[
W_{DA}=-p_0 V_0
\] 以上より,正味の仕事 \(W_{total}\) は \[
W_{total}=2p_0 V_0-p_0 V_0=p_0 V_0
\]
補足
(2) の結果から,p-V グラフで囲まれた部分の面積は気体のする仕事を表していることがわかります。
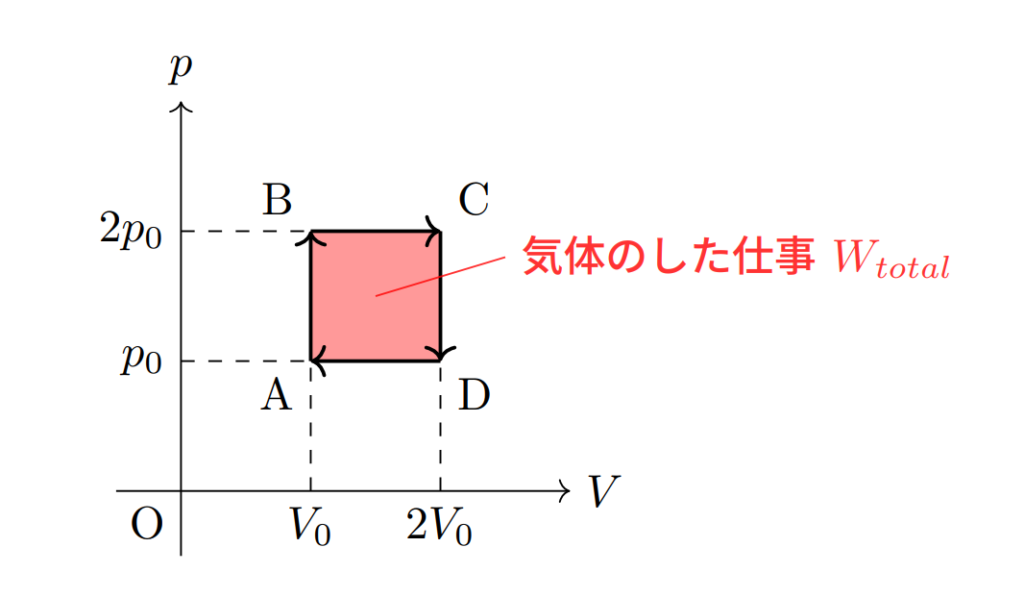
この事実は一般化することが可能で,これは次のように書くことが出来ます。
系内部の圧力を \(p\) 変化前後の体積を \(V_1,V_2\) とすると気体のする仕事 \(W\) は \[W=\int_{V_1}^{V_2}pdV\] である。
(3) の考え方
(1) で得た各点の温度と,内部エネルギーの関係式 $\displaystyle U=\frac32 nRT$ を用いてエネルギー変化を求めましょう。
【解答】
各点における内部エネルギーを求める。(1) より \[
T_B=2T_0,\;T_C=4T_0,\;T_D=2T_0
\] であることを用いると A,B,C,D の内部エネルギーは \[
U_A=\frac{3}{2}nRT_0,\quad U_B=3nRT_0 \\U_C=6nRT_0,\quad U_D=3nRT_0
\] これより各過程の内部エネルギー変化は気体の状態方程式 \(p_0 V_0 =nRT_0\) も使って \[
\begin{align}
d U_{AB}=\frac{3}{2}p_0 V_0 &\quad d U_{BC}=3p_0 V_0 \\
d U_{AB}=-3p_0 V_0 &\quad d U_{AB}=\frac{3}{2}p_0 V_0 \end{align}
\] である。
(4)の考え方
内部エネルギーの変化が求まったので,熱力学第1法則を使って気体が得た熱量を求めます。尚,熱力学第1法則は気体が得た熱量を \(d’ Q\),気体がした仕事を \(d’W\),気体の内部エネルギー変化を \(d U\) とすると \[
dU=d’Q-d’W
\] で書くことが出来ますね。$Q$ の符号に注意しましょう(本問では気体が得た熱量と,外部にした仕事が正としています)。
【解答】
A→Bにおいて \( W_{AB}=0\),\(\displaystyle d U_{AB}=\frac{3}{2}p_0 V_0\) より,気体が得た熱量は \[
Q_{AB}=+\frac{3}{2}p_0 V_0
\] B→Cにおいて \( W_{BC}=2p_0 V_0\),\(\displaystyle d U_{BC}=3p_0 V_0\) より,気体が得た熱量は \[
Q_{BC}=+5p_0 V_0
\] C→Dにおいて \( W_{CD}=0\),\(\displaystyle d U_{CD}=-3p_0 V_0\) より,気体が得た熱量は \[
Q_{CD}=\color{red}{-}3p_0 V_0
\] D→Aにおいて \( W_{DA}=p_0 V_0\),\(\displaystyle d U_{DA}=-\frac{3}{2}p_0 V_0\) より,気体が得た熱量は \[
Q_{DA}=\color{red}{-}\frac{1}{2}p_0 V_0
\]
(5) の考え方
熱効率 \(e\) は \[e=\frac{W_{total}}{Q_{in}}\] で定義されます。ここで熱効率の分母における \(Q_{in}\) は「気体が得た正の熱量」であって系が得た正味の熱量 \(Q_{total}\) ではないことに注意しましょう。ここで系が得た熱量は \(Q>0\) の部分の和,すなわち \[\begin{align} Q_{in} &= Q_{AB}+Q_{BC}\\ &=5p_0 V_0+\frac{3}{2}p_0 V_0\\ &=\frac{13}{2}p_0 V_0 \end{align}\] と計算することが出来ます。
【解答】
気体がした正味の仕事 \(W_{total}=p_0 V_0\),気体が得た正味の熱量 \(\displaystyle Q=\frac{13}{2}p_0 V_0\) より,この熱機関の熱効率 \(e\) は \[
e=\frac{W_{total}}{Q}=\frac{2}{13}
\] である。


コメント